UFAM 2013
Uma estudante fez um experimento para determinar a variação de entalpia, ΔH, de uma reação química. Ela adicionou excesso de zinco sólido a 25,00 mL de uma solução de sulfato de cobre (1,00 mol L-1) em um calorímetro de garrafa de café, agitou a mistura e mediu o aumento da temperatura, que foi de 49,8 oC. Levou cerca de 90 segundos para que esta temperatura fosse atingida. Ela então calculou o resultado usando a expressão:
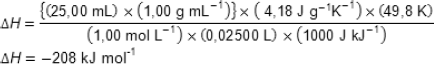
O valor da literatura é –217 kJ mol–1. Qual das seguintes observações NÃO contribuiu para o erro no resultado da estudante?
A densidade da solução é maior do que a da água.
A capacidade de calor da solução é maior do que a da água.
A capacidade de calor do excesso de zinco não foi incluída no cálculo.
O tempo necessário para a temperatura se elevar ao máximo foi considerado.
A capacidade de calor do termômetro não foi incluída no cálculo.
E mais: nota TRI a todo o momento.





