EsPCEx 2017
“Sempre que uma substância muda de fase de agregação, a temperatura permanece constante enquanto a mudança se processa, desde que a pressão permaneça constante”.
FONSECA Martha Reis Marques da, Química Geral, São Paulo: Ed FTD, 2007, pág 41.
O gráfico abaixo representa a mudança de fase de agregação de uma substância pura com o passar do tempo, em função da variação de temperatura, observada ao se aquecer uma substância X durante algum tempo, sob pressão constante.
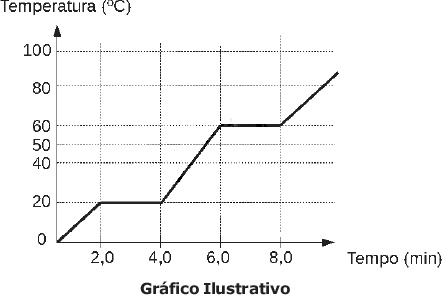
Tomando-se como base o gráfico, analise as seguintes afirmativas:
I – entre 0 ºC e 19 ºC, a substância X encontra-se na fase sólida;
II – o intervalo de 2,0 min a 4,0 min corresponde à condensação da substância X;
III – a temperatura de 60 ºC corresponde à temperatura de ebulição da substância X;
IV – no intervalo de 40 ºC a 50 ºC, a substância X encontra-se na fase líquida.
Estão corretas apenas as afirmativas
I e II.
II e IV.
I, II e III.
II, III e IV.
I, III e IV
E mais: nota TRI a todo o momento.





