
UEA 2023
Para ilustrar o modelo atômico de Bohr, um professor de Física propõe uma atividade em que circunferências concêntricas desenhadas no chão representam os níveis de energia do átomo de hidrogênio, conforme a figura.
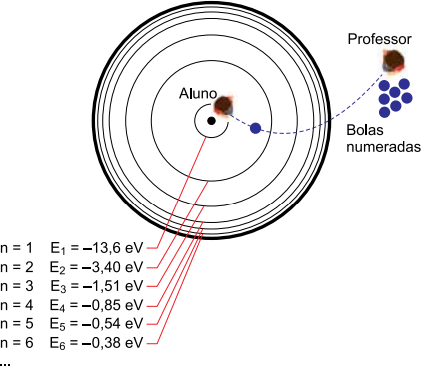
Um aluno, fazendo o papel do elétron ligado ao átomo, posiciona-se sobre uma das circunferências. Assim como o elétron, o aluno possuirá energia correspondente ao nível de energia da circunferência na qual se encontra. O professor de Física posiciona-se do lado de fora das circunferências e lança bolas numeradas com valores de energia, em eV, para o aluno. Ao conseguir apanhar uma bola, que simboliza um fóton, o aluno deve conferir o valor de energia numerado na bola e saltar diretamente para a circunferência que equivale ao seu saldo de energia.
Suponha que o aluno esteja na circunferência de n = 2 e apanhe uma bola numerada com 2,86 eV. Nesse momento, ele deverá saltar imediatamente para a circunferência de
n = 3.
n = 6.
n = 5.
n = 4.
n = 1.
Insights de Estudo
Taxa de Acerto
Material de Estudo
Conteúdo Exclusivo
Cadastre-se para ver dicas, estratégias e análise completa desta questão
Criar conta grátis →🎓 AIO + UEA: Preparação Baseada em Dados
Fizemos o trabalho difícil para você não ter que fazer
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de AI + aprendizado ativo


