
UnB 2019
Para aumentar a velocidade da reação de síntese do NH3(g), pode-se utilizar como catalisador pó de ferro finamente dividido. Os reagentes, N2(g) e H2(g), podem ser obtidos a partir do ar atmosférico e da reforma do metano, respectivamente. Após a reação, a lavagem do sistema com água permite separar o NH3 do N2(g) e do H2(g) remanescentes.
Devido à sua volatilidade, o NH3 é usualmente convertido em ureia (H2NCONH2) ou em nitrato de amônio (NH4NO3), o que pode ser feito por meio das reações com CO2(g) e HNO3(g), respectivamente.
A lei de velocidade para a reação de síntese do NH3(g) a partir de N2(g) e H2(g) é de ordem global 2, sendo de ordem 1 em relação a cada um dos reagentes.
Considerando as informações e condições apresentadas e assumindo comportamento ideal para todos os gases envolvidos, julgue o item.
Considere que a síntese de NH3(g) seja realizada em um sistema que contém, inicialmente, apenas N2(g) e H2(g) em determinadas concentrações iniciais. Nessas condições, utilize o sistema de eixos abaixo fornecido para esboçar duas curvas da concentração de NH3 em função do tempo de reação até ser atingido o equilíbrio químico; uma curva (em linha cheia) deve representar a reação catalisada e, a outra (em linha tracejada), a reação não catalisada.
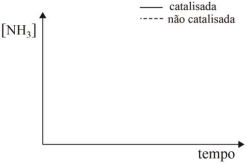
O gráfico acima é de uso opcional, para rascunho. Não se esqueça de transferir a sua resposta para o Caderno de Respostas.
Insights de Estudo
Taxa de Acerto
Material de Estudo
Conteúdo Exclusivo
Cadastre-se para ver dicas, estratégias e análise completa desta questão
Criar conta grátis →🎓 AIO + UnB: Preparação Baseada em Dados
Fizemos o trabalho difícil para você não ter que fazer
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de AI + aprendizado ativo


