USF 2019/2
Os ácidos inorgânicos possuem inúmeras aplicações em nosso cotidiano e também nas indústrias. O fósforo é um elemento que propicia a formação de vários desses ácidos, sendo que o ácido fosfórico, cuja estrutura está apresentada a seguir, é o mais importante deles. Suas aplicações variam desde conservante de bebidas refrigerantes até utilização como substância que remove a ferrugem de peças metálicas.
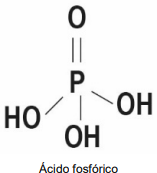
A partir das informações propiciadas pela análise da estrutura molecular de uma molécula de ácido fosfórico, avalie as afirmativas a seguir e assinale a correta.
Dados valores de número atômico: H = 1; O = 8; P = 15 e K = 19.
O átomo de fósforo assume geometria molecular do tipo piramidal.
Ainda que seja classificada como ácido, essa substância possui caráter alcalino devido à presença dos grupos hidroxila.
O número de oxidação do fósforo na formação desse ácido é -3.
Uma reação de neutralização total desse ácido com a base hidróxido de potássio necessitaria de um mol do ácido para cada três mols da base.
As interações das moléculas desse ácido com as moléculas de água ocorrem por forças do tipo dipolo-induzido.
E mais: nota TRI a todo o momento.





