
PUC-PR Verão Medicina 2016
O Princípio de Le Chatelier infere que quando uma perturbação é imposta a um sistema químico em equilíbrio, este irá se deslocar de forma a minimizar tal perturbação.
Disponível em: brasilescola.com/exercicios-quimica/exercicios-sobre-principio-le-chatelier.htm
O gráfico apresentado a seguir indica situações referentes à perturbação do equilíbrio químico indicado pela equação H2(g) + I2(g) ⇌ 2 HI(g)
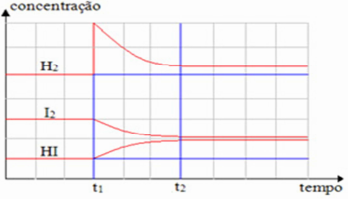
A partir da equação química apresentada e da observação do gráfico, considerando também que a reação é endotérmica em favor da formação do ácido iodídrico, a dinâmica do equilíbrio favorecerá
a formação de iodo quando da adição de gás hidrogênio.
a diminuição na quantidade de ácido iodídrico quando do aumento da temperatura.
o aumento na quantidade das substâncias simples quando ocorrer elevação da pressão total do sistema.
formação de gás hidrogênio na reação direta a partir de t1, em virtude da adição de ácido iodídrico.
o consumo de iodo quando da adição de gás hidrogênio.
Insights de Estudo
Taxa de Acerto
Material de Estudo
Conteúdo Exclusivo
Cadastre-se para ver dicas, estratégias e análise completa desta questão
Criar conta grátis →🎓 AIO + PUC-PR: Preparação Baseada em Dados
Fizemos o trabalho difícil para você não ter que fazer
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de AI + aprendizado ativo


