UESB Caderno 3 2011
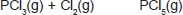
O pentacloreto de fósforo, PCl5(g), pode ser obtido a partir do equilíbrio químico, representado pela equação química, quando, em um recipiente de 3,0L, a 200oC, fechado, está presente em uma mistura contendo 0,600mol de PCl3(g), 0,120mol de Cl2(g) e 0,120mol de PCl5(g).
De acordo com essas informações, é correto afirmar:
A concentração de PCl5(g), no equilíbrio químico, é 0,120 mol.L−1.
A diminuição da concentração de Cl2(g) no sistema provoca aumento da concentração de PCl5(g).
A constante de equilíbrio, Keq, para essa reação é igual a, aproximadamente, 5,0mol−1L.
O valor da constante de equilíbrio, Keq, se mantém inalterado com a variação de temperatura do recipiente.
A adição de um catalisador à mistura reagente provoca aumento da concentração de PCl5(g) no sistema em equilíbrio químico.
E mais: nota TRI a todo o momento.





