UNIFOR Bacharelado 2018
O modelo atômico de Rutherford foi fundamentado nas observações do experimento em que uma fina lâmina de ouro (0,0001 mm de espessura) foi bombardeada com partículas alfa, emitidas pelo polônio (Po) contido no interior de um bloco de chumbo (Pb), provido de uma abertura estreita, para dar passagem às partículas por ele emitidas. Envolvendo a lâmina de ouro (Au), foi colocada uma tela protetora revestida de sulfeto de zinco, conforme figura abaixo.
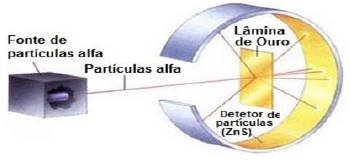
Observando as cintilacões na tela revestida de sulfeto de zinco, Rutherford verificou que muitas partículas atravessavam a lâmina de ouro sem sofrer desvio e que poucas partículas sofriam desvio.
De acordo com o experimento de Rutherford, está correto o que se afirma em:
As partículas α sofrem desvio ao colidir com os núcleos dos átomos de Au.
As partículas α possuem carga elétrica negativa.
Partículas α sofrem desvio ao colidir com elétrons dos átomos de Au.
Na ilustracão, não foram indicadas as partículas α que não atravessaram a lâmina de Au.
O tamanho do átomo é cerca de 1.000 a 10.000 vezes maior que o seu núcleo.
E mais: nota TRI a todo o momento.





