clear
UEG 2015/1
O gráfico a seguir representa a variação de entalpia para uma reação genérica que pode levar à formação dos produtos P1 e P2 a partir do reagente R.
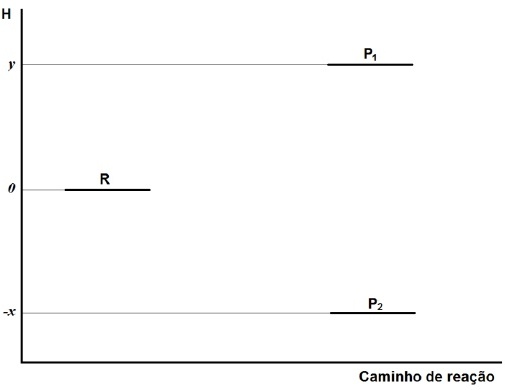
A análise do gráfico permite concluir que a
a
reação libera energia para produção de P1.
b
produção de P2 é um processo endotérmico.
c
variação de entalpia para formação de P1 é y.
d
reação que leva a P2 ocorre com maior rendimento.
Ver resposta
Ver resposta
Resposta
C
Tempo médio
45 s
Resolução
Assine a AIO para ter acesso a esta e muitas outras resoluções
Mais de 300.000 questões com resoluções e dados exclusivos disponíveis para alunos AIO.
E mais: nota TRI a todo o momento.
E mais: nota TRI a todo o momento.
Saiba mais
Esta resolução não é pública. Assine a aio para ter acesso a essa resolução e muito mais:
Tenha acesso a simulados reduzidos, mais de 200.000 questões, orientação personalizada,
video aulas, correção de redações e uma equipe sempre disposta a te ajudar.
Tudo isso com acompanhamento TRI em tempo real.
Dicas
expand_more
expand_less
Dicas sobre como resolver essa questão
Erros Comuns
expand_more
expand_less
Alguns erros comuns que estudantes podem cometer ao resolver esta questão
Conceitos chave
Conceitos chave sobre essa questão, que pode te ajudar a resolver questões similares
Estratégia de resolução
Uma estratégia sobre a forma apropriada de se chegar a resposta correta
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de
AI + aprendizado ativo.
+25 pts
Aumento médio TRI
4x
Simulados mais rápidos
+50 mil
Estudantes

Débora Adelina
O que mais gostei foi a forma como a plataforma seleciona matérias em que tenho mais dificuldade, ajudando a focar no que realmente preciso de atenção. Ainda não consegui minha aprovação, mas contarei com a AIO por mais um ano pois a plataforma me aproximou desse objetivo tornando meus estudos mais direcionados!

Joice Neves
Faltavam 3 meses para o ENEM, eu estava desesperada e mentalmente fragilizada por não ver os resultados do meu esforço. Então, eu encontrei a AIO e, em 3 meses, eu consegui aumentar a minha nota média em 50 pontos. Meses depois, fui aprovada no curso que eu tanto desejei. Esse sonho se tornou real graças à AIO.

Jonas de Souza
As correções de redações e as aulas são bem organizadas e é claro os professores são os melhores com a melhor metodologia de ensino, sem dúvidas contribuiu muito para o aumento de 120 pontos na minha média final!


