FPP Inverno Medicina 2017
O gráfico a seguir apresenta as solubilidades de alguns sais de acordo com a variação da temperatura.
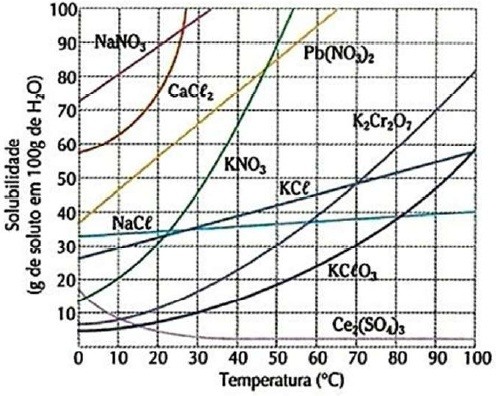
Mais do que apenas avaliar se determinada substância é razoavelmente solúvel em um determinado solvente a uma dada temperatura o estudo das solubilidades das substâncias é bastante relevante bioquimicamente, pois está associado a inúmeros fatores como, por exemplo, a retenção de líquidos em determinadas circunstâncias. A avaliação do gráfico apresentado permite concluir que:
(Considere que a densidade da água é de 1 g/cm3).
a 40° C a dissolução de aproximadamente 65 g de nitrato de potássio satura uma solução que foi preparada com essa massa de sal em 100 mL de água;
a 40° C a dissolução de aproximadamente 40 g de cloreto de sódio em 100 mL de água torna a solução insaturada por apresentar mais sal dissolvido do que o coeficiente de solubilidade estabelece para essa temperatura;
a 70° C percebe-se que cloreto de potássio e o dicromato de potássio apresentam a mesma solubilidade em 100 mL de água dessa forma essas soluções apresentarão também o mesmo valor de concentração molar;
o sulfato de cério II é a única substância que possui dissolução endotérmica em meio aquoso;
no geral as solubilidades das substâncias são aumentadas com a elevação da temperatura, algo que não se reflete ao avaliar o ponto de ebulição das soluções aquosas de sais que diminuem com a presença dessas substâncias.
E mais: nota TRI a todo o momento.





