
ENEM 2019 segunda aplicação
O gás hidrogênio é considerado um ótimo combustível — o único produto da combustão desse gás é o vapor de água, como mostrado na equação química.
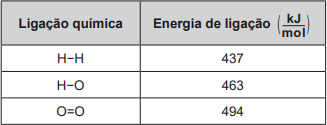
Um cilindro contém 1 kg de hidrogênio e todo esse gás foi queimado. Nessa reação, são rompidas e formadas ligações químicas que envolvem as energias listadas no quadro.
Massas molares \( \frac{g}{mol}: H_2 = 2; O_2 = 32; H_2O = 18 \)
Qual é a variação da entalpia, em quilojoule, da reação de combustão do hidrogênio contido no cilindro?
\(-242,000\)
\(-121,000\)
\(-2.500\)
\(+110500\)
Caracterizar materiais ou substâncias, identificando etapas, rendimentos ou implicações biológicas, sociais, econômicas ou ambientais de sua obtenção ou produção.
Insights de Estudo
Taxa de Acerto
Material de Estudo
Conteúdo Exclusivo
Cadastre-se para ver dicas, estratégias e análise completa desta questão
Criar conta grátis →🎯 AIO + ENEM: A TRI Mais Precisa do Brasil
até 99,9% de precisão na nota TRI
Aprendizado Personalizado com TRI + AI
-
✓Identifica sua nota real em cada área
Precisão de 99,9% para as provas Enem até 2024
-
✓Recomenda questões no seu nível
IA ajusta a dificuldade ao seu desempenho
-
✓Mostra seu progresso em tempo real
Acompanhe sua evolução com métricas precisas
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de AI + aprendizado ativo


