
UNIFAE 2015
O ferro é o metal mais utilizado na indústria, mas quando exposto ao ar úmido sofre corrosão. A reação de formação do óxido de ferro hidratado, mais conhecido como ferrugem, é apresentada a seguir.
4Fe2+(aq) + O2(g) + (4 + 2x) H2O(ℓ) → 2Fe2O3 ⋅ xH2O(s) + 8 H+(aq)
Um dos modos de se proteger o ferro da corrosão é revesti-lo com outro metal. A figura mostra um pedaço de ferro revestido de zinco, já com alguns sinais de corrosão da camada protetora.
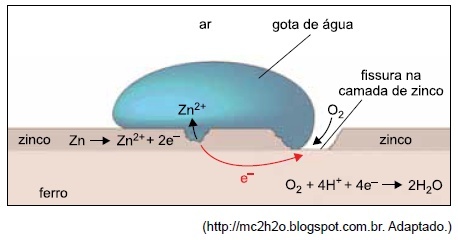
Considere os potenciais de redução do ferro, do zinco e do oxigênio:
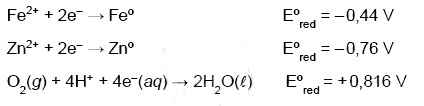
o zinco é o cátodo nesse processo.
durante o processo descrito ocorre diminuição da massa de zinco e formação de Fe2+.
a fissura na camada de zinco provocará oxidação do ferro.
o zinco atua como metal de sacrifício.
o zinco, por ter menor Eºred, sofre redução e por isso ocorre a fissura.
Insights de Estudo
Taxa de Acerto
Material de Estudo
Conteúdo Exclusivo
Cadastre-se para ver dicas, estratégias e análise completa desta questão
Criar conta grátis →🎓 AIO + UNIFAE: Preparação Baseada em Dados
Fizemos o trabalho difícil para você não ter que fazer
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de AI + aprendizado ativo


