
Unaerp 2014/2
O experimento a seguir foi feito com as substâncias: água, etanol e éter e mostra a diferença nas pressões de vapor dos líquidos após certo tempo.
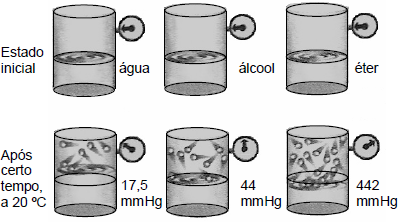
FELTRE, R. Química Geral. Vol 1. 7 ed. São Paulo: Ed. Moderna, 2008. p. 337.
Com base na figura e considerando a relação entre a pressão de vapor dos líquidos com seus pontos de ebulição, são feitas as seguintes afirmações.
1. A pressão de vapor é maior no frasco contendo éter, devido a seu maior ponto de ebulição.
2. As três substâncias têm interação intermolecular por pontes de hidrogênio.
3. A água tem menor pressão de vapor, porque faz pontes de hidrogênio, o que eleva seu ponto de ebulição.
4. As pressões indicadas pelos manômetros são exercidas pelas partículas das substâncias que se transformaram em vapor e, quando se trata de líquidos, está relacionada com a intensidade de suas interações intermoleculares.
Somente 1 e 3 estão corretas.
Somente 1 e 4 estão corretas.
Somente 1, 2 e 3 estão corretas.
Somente 3 e 4 estão corretas.
1, 2, 3 e 4 estão corretas.
Insights de Estudo
Taxa de Acerto
Material de Estudo
Conteúdo Exclusivo
Cadastre-se para ver dicas, estratégias e análise completa desta questão
Criar conta grátis →🎓 AIO + Unaerp: Preparação Baseada em Dados
Fizemos o trabalho difícil para você não ter que fazer
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de AI + aprendizado ativo


