
ENEM digital 2020
O elemento ferro é essencial em nossa alimentação, pois ajuda a prevenir doenças como a anemia. Normalmente, na alimentação é ingerido na forma de Fe3+, sendo necessário o uso de agentes auxiliares de absorção, como o ácido ascórbico (vitamina C), cuja ação pode ser representada pelo esquema reacional a seguir.
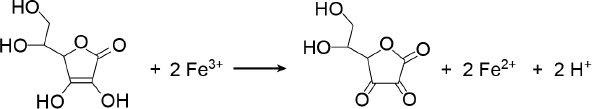
A ação do ácido ascórbico ocorre por meio de uma reação de
eliminação.
substituição.
oxirredução.
neutralização.
hidrogenação.
Utilizar códigos e nomenclatura da química para caracterizar materiais, substâncias ou transformações químicas.

Insights de Estudo
Taxa de Acerto
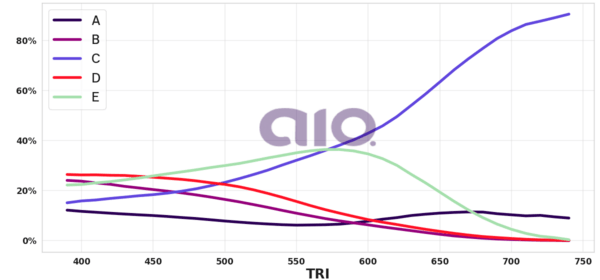
Distribuição TRI

Faça login para ver
análise completa
Material de Estudo
Conteúdo Exclusivo
Cadastre-se para ver dicas, estratégias e análise completa desta questão
Criar conta grátis →🎯 AIO + ENEM: A TRI Mais Precisa do Brasil
até 99,9% de precisão na nota TRI
Aprendizado Personalizado com TRI + AI
-
✓Identifica sua nota real em cada área
Precisão de 99,9% para as provas Enem até 2024
-
✓Recomenda questões no seu nível
IA ajusta a dificuldade ao seu desempenho
-
✓Mostra seu progresso em tempo real
Acompanhe sua evolução com métricas precisas
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de AI + aprendizado ativo


