
UFN Verão 2009/2
O composto NaHCO3:
- é um antiácido estomacal, pois neutraliza o excesso de HCl no suco gástrico.
Reação I
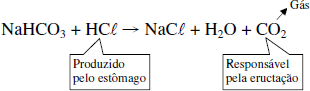
- é o principal componente do alka-seltzer, sonrisal, sal de frutas eno etc..., que contêm também ácidos orgânicos sólidos, como o ácido tartárico, o cítrico e outros (representados genericamente por R – COOH). Na presença da água ocorre a reação
Reação II
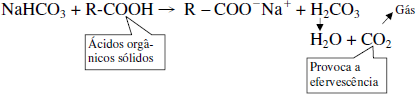
- é utilizado na produção de fermentos para pães, bolos, biscoitos etc., porque, quando é aquecido, há liberação de CO2(gás) que faz a massa crescer.
Reação III
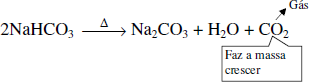
- é utilizado também na fabricação de extintores de incêndio à base de espuma, onde o NaHCO3 sólido e o H2SO4 em solução são colocados em compartimentos separados. Quando o extintor é acionado, o NaHCO3 mistura-se com o H2SO4 e a reação produz CO2, que apaga o fogo.
Reação IV
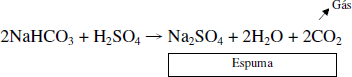
De acordo com o texto acima, qual a proposição incorreta?
O acido da reação I é denominado acido clorídrico e o da reação IV, ácido sulfúrico, sendo ambos classificados, quanto ao seu grau de ionização, como ácidos fortes.
A reação II é classificada como reação de dupla troca e a III, como reação de análise ou decomposição.
Os sais formados nas reações I, III e IV são denominados, respectivamente, cloreto de sódio, carbonato de sódio e sulfato de sódio, sendo os três classificados como sais normais.
O NaHCO3 é classificado como sal ácido ou hidrogeno-sal, denominado carbonato de sódio, e o óxido gasoso produzido nas reações I, II, III e IV, a partir dele, é classificado como óxido ácido.
Os extintores que utilizam o NaHCO3 (espuma) não podem ser usados para apagar fogo de instalações elétricas, pois a espuma é eletrolítica, isto é, conduz a corrente elétrica, sendo usados, portanto, em chamas provocadas por líquidos inflamáveis.
Insights de Estudo
Taxa de Acerto
Material de Estudo
Conteúdo Exclusivo
Cadastre-se para ver dicas, estratégias e análise completa desta questão
Criar conta grátis →🎓 AIO + UFN: Preparação Baseada em Dados
Fizemos o trabalho difícil para você não ter que fazer
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de AI + aprendizado ativo


