
USF 2013
USF
📚
+
1.060
questões USF
Comece sua preparação
→
USF 2013/2
O ciclamato de sódio é uma substância bastante utilizada como adoçante artificial em vários alimentos e bebidas. Um famoso suco de frutas em pó possui concentração comum de 100 mg de ciclamato de sódio para cada 100 mL de solução aquosa. Considerando a estrutura molecular do ciclamato de sódio apresentada a seguir, analise as afirmações.
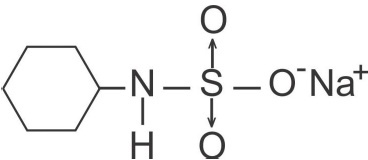
• Dados os valores das massas atômicas em g/mol: H = 1,0; C = 12,0; N = 14,0; O = 16,0; Na = 23,0 e S = 32,0.
• Observação: para efeito do cálculo da massa molecular não considere os sinais positivo e negativo nos átomos de oxigênio e sódio. As flechas indicam ligações coordenadas e os traços são ligações covalentes normais e também não influenciam no cálculo da massa molecular.
I. A solução aquosa desse composto deve possuir uma temperatura de congelamento inferior à da água pura.
II. Trata-se de um composto aromático.
III. A concentração molar dessa solução é de aproximadamente 0,005 mols/L.
IV. A concentração comum dessa solução é de aproximadamente 10 g/L.
V. A concentração molar dessa solução é de aproximadamente 0,000005 mols/L.
Dentre as afirmações realizadas, estão corretas apenas
• Observação: para efeito do cálculo da massa molecular não considere os sinais positivo e negativo nos átomos de oxigênio e sódio. As flechas indicam ligações coordenadas e os traços são ligações covalentes normais e também não influenciam no cálculo da massa molecular.
I. A solução aquosa desse composto deve possuir uma temperatura de congelamento inferior à da água pura.
II. Trata-se de um composto aromático.
III. A concentração molar dessa solução é de aproximadamente 0,005 mols/L.
IV. A concentração comum dessa solução é de aproximadamente 10 g/L.
V. A concentração molar dessa solução é de aproximadamente 0,000005 mols/L.
Dentre as afirmações realizadas, estão corretas apenas
a
I, II e III.
b
I e III.
c
II e III.
d
II e V.
e
I e IV.
Resposta
B
Tempo médio
3 min
Resolução
Esta resolução não é pública. Assine a aio para ter acesso a essa resolução e muito mais:
Tenha acesso a simulados reduzidos, mais de 200.000 questões, orientação personalizada,
video aulas, correção de redações e uma equipe sempre disposta a te ajudar.
Tudo isso com acompanhamento TRI em tempo real.
Dicas
expand_more
expand_less
Dicas sobre como resolver essa questão
Erros Comuns
expand_more
expand_less
Alguns erros comuns que estudantes podem cometer ao resolver esta questão
Conceitos chave
Conceitos chave sobre essa questão, que pode te ajudar a resolver questões similares
Estratégia de resolução
Uma estratégia sobre a forma apropriada de se chegar a resposta correta
✓
Resposta Correta
B
Dificuldade
Média
• 61% acertaram
Tempo Médio
3min 41s
📊
Insights de Estudo
⚗️
Funções orgânicas
•
Química
Taxa de Acerto
61%
acerto
💡
Material de Estudo
🔓
Conteúdo Exclusivo
Cadastre-se para ver dicas, estratégias e análise completa desta questão
Criar conta grátis →
🎓
Vestibular
🎓 AIO + USF: Preparação Baseada em Dados
Fizemos o trabalho difícil para você não ter que fazer
📚
1.060
questões USF
📊
24%
cobertura de tópicos
🎯
0
alunos prep. para USF
⭐
Depoimentos
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de AI + aprendizado ativo
+25 pts
Aumento médio TRI
4x
Simulados mais rápidos
+80 mil
Estudantes

Mariana Scheffel
Aprovado
❝
AIO foi fundamental para a evolução do meu número de acertos e notas, tanto no ENEM quanto em outros vestibulares, fornecendo os recursos e as ferramentas necessárias para estudar de forma eficaz e melhorar minhas notas.

Sarah
Aprovado
❝
Neste ano da minha aprovação, a AIO foi a forma perfeita de eu entender meus pontos fortes e fracos, melhorar minha estratégia de prova e, alcançar uma nota excepcional que me permitiu realizar meu objetivo na universidade dos meus sonhos. Só tenho a agradecer à AIO ... pois com certeza não conseguiria sozinha.

Jairo Thiago
Aprovado
❝
Conheci a plataforma através de uma reportagem e, como gosto de IA, resolvi investir. A quantidade de questões e suas análises foram tão boas que meu número de acertos foi o suficiente para entrar em Medicina na Federal do meu estado, só tenho que agradecer à equipe do AIO pela minha tão sonhada aprovação!