
UnB 2018
UnB
📚
+
9.030
questões UnB
Comece sua preparação
→
UnB 2018
No experimento retratado, Lavoisier colocou mercúrio puro aquecido em uma retorta (A), com um longo tubo (B) ligado a uma redoma (E), contendo ar, em um recipiente que também contém mercúrio (R). Durante 12 dias aqueceu a retorta, que estava sobre um forno (N), notou que um óxido vermelho de mercúrio se formava. Quando não havia mais pó vermelho formado, Lavoisier observou que cerca de um quinto do ar na redoma havia sido utilizado e que o gás remanescente não suportava a vida ou a queima. Lavoisier chamou este de azote (Do grego 'a' e 'zoe' = sem vida). Ele removeu o óxido vermelho de mercúrio, com cuidado, e aqueceu-o em uma retorta semelhante, obtendo exatamente o mesmo volume de gás que desaparecera no último experimento. Ele descobriu que este gás fazia as chamas queimarem brilhantemente, e pequenos animais estavam ativos nele, como Joseph Priestley notara em seu experimento. Finalmente, ao misturar os dois tipos de gás, ou seja, o gás restante na primeira experiência, e o que fora conseguido no segundo experimento, ele obteve uma mistura semelhante ao ar em todos os aspectos. Em seus experimentos, Lavoisier analisou o ar em dois constituintes: um que sustenta a vida e a combustão, e era equivalente a um quinto em volume de ar, que ele chamou de oxigênio (grego, oxus = ácido, gen = gera), e os outros quatro quintos, que ele chamou de azote. Este último gás é, agora, chamado de nitrogênio.
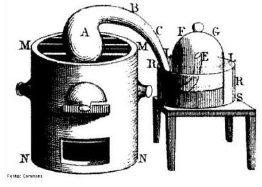


Acerca do assunto tratado no texto e do próprio texto, julgue o item:
O mesmo óxido vermelho de mercúrio obtido na reação executada por Lavoisier pode ser obtido a partir da pirólise do nitrato de mercúrio.

a
Certo.
b
Errado.
Resposta
A
Tempo médio
2 min
Resolução
Esta resolução não é pública. Assine a aio para ter acesso a essa resolução e muito mais:
Tenha acesso a simulados reduzidos, mais de 200.000 questões, orientação personalizada,
video aulas, correção de redações e uma equipe sempre disposta a te ajudar.
Tudo isso com acompanhamento TRI em tempo real.
Dicas
expand_more
expand_less
Dicas sobre como resolver essa questão
Erros Comuns
expand_more
expand_less
Alguns erros comuns que estudantes podem cometer ao resolver esta questão
Conceitos chave
Conceitos chave sobre essa questão, que pode te ajudar a resolver questões similares
Estratégia de resolução
Uma estratégia sobre a forma apropriada de se chegar a resposta correta
✓
Resposta Correta
A
Dificuldade
Muito Difícil
• 0% acertaram
Tempo Médio
2min 50s
📊
Insights de Estudo
⚗️
Reações inorgânicas
•
Química
Taxa de Acerto
0%
acerto
💡
Material de Estudo
🔓
Conteúdo Exclusivo
Cadastre-se para ver dicas, estratégias e análise completa desta questão
Criar conta grátis →
🎓
Vestibular
🎓 AIO + UnB: Preparação Baseada em Dados
Fizemos o trabalho difícil para você não ter que fazer
📚
9.030
questões UnB
📊
36%
cobertura de tópicos
🎯
0
alunos prep. para UnB
⭐
Depoimentos
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de AI + aprendizado ativo
+25 pts
Aumento médio TRI
4x
Simulados mais rápidos
+80 mil
Estudantes

Mariana Scheffel
Aprovado
❝
AIO foi fundamental para a evolução do meu número de acertos e notas, tanto no ENEM quanto em outros vestibulares, fornecendo os recursos e as ferramentas necessárias para estudar de forma eficaz e melhorar minhas notas.

Débora Adelina
Aprovado
❝
O que mais gostei foi a forma como a plataforma seleciona matérias em que tenho mais dificuldade, ajudando a focar no que realmente preciso de atenção. Ainda não consegui minha aprovação, mas contarei com a AIO por mais um ano pois a plataforma me aproximou desse objetivo tornando meus estudos mais direcionados!

Jairo Thiago
Aprovado
❝
Conheci a plataforma através de uma reportagem e, como gosto de IA, resolvi investir. A quantidade de questões e suas análises foram tão boas que meu número de acertos foi o suficiente para entrar em Medicina na Federal do meu estado, só tenho que agradecer à equipe do AIO pela minha tão sonhada aprovação!