clear
UFRR 2015
Credita-se ao russo Dmitri Mendeleev o mérito de ter elaborado a primeira versão da tabela periódica. Desde então, muitas foram as contribuições até se chegar a atual tabela, um dos instrumentos de consulta mais utilizados pelos químicos e estudantes de Química de todo o mundo. Em relação à classificação periódica atual, conforme tabela a seguir, analise as seguintes proposições:
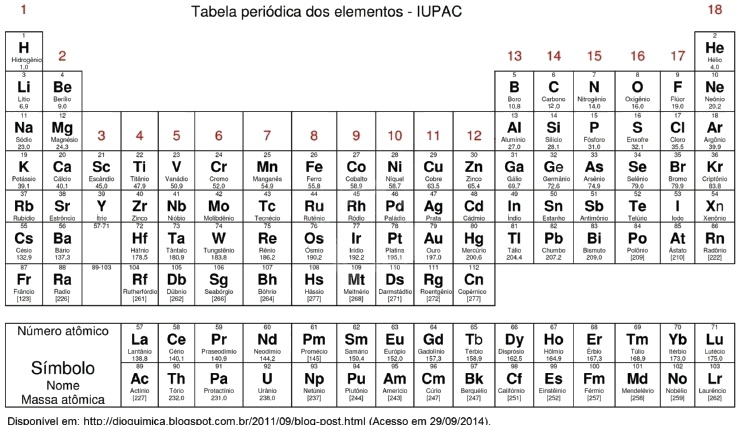
I - os elementos são listados em ordem crescente de número atômico;
II - os elementos de um mesmo período têm configurações eletrônicas da camada de valência semelhantes e, portanto, propriedades químicas semelhantes;
III - para uma série de elementos de transição pertencente ao mesmo período e dispostos em ordem crescente de número atômico, os elétrons vão sendo acrescentados sucessivamente à penúltima camada eletrônica;
IV - em um período ou grupo, a energia de ionização tende a ser tanto maior quanto menor for o raio atômico.
Estão corretas:
II - os elementos de um mesmo período têm configurações eletrônicas da camada de valência semelhantes e, portanto, propriedades químicas semelhantes;
III - para uma série de elementos de transição pertencente ao mesmo período e dispostos em ordem crescente de número atômico, os elétrons vão sendo acrescentados sucessivamente à penúltima camada eletrônica;
IV - em um período ou grupo, a energia de ionização tende a ser tanto maior quanto menor for o raio atômico.
Estão corretas:
a
II – III – IV;
b
I – II;
c
I – IV;
d
I– III – IV;
e
III – IV.
Ver resposta
Ver resposta
Resposta
D
Tempo médio
1 min
Resolução
Assine a AIO para ter acesso a esta e muitas outras resoluções
Mais de 300.000 questões com resoluções e dados exclusivos disponíveis para alunos AIO.
E mais: nota TRI a todo o momento.
E mais: nota TRI a todo o momento.
Saiba mais
Esta resolução não é pública. Assine a aio para ter acesso a essa resolução e muito mais:
Tenha acesso a simulados reduzidos, mais de 200.000 questões, orientação personalizada,
video aulas, correção de redações e uma equipe sempre disposta a te ajudar.
Tudo isso com acompanhamento TRI em tempo real.
Dicas
expand_more
expand_less
Dicas sobre como resolver essa questão
Erros Comuns
expand_more
expand_less
Alguns erros comuns que estudantes podem cometer ao resolver esta questão
Conceitos chave
Conceitos chave sobre essa questão, que pode te ajudar a resolver questões similares
Estratégia de resolução
Uma estratégia sobre a forma apropriada de se chegar a resposta correta
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de
AI + aprendizado ativo.
+25 pts
Aumento médio TRI
4x
Simulados mais rápidos
+50 mil
Estudantes

Débora Adelina
O que mais gostei foi a forma como a plataforma seleciona matérias em que tenho mais dificuldade, ajudando a focar no que realmente preciso de atenção. Ainda não consegui minha aprovação, mas contarei com a AIO por mais um ano pois a plataforma me aproximou desse objetivo tornando meus estudos mais direcionados!

Jairo Thiago
Conheci a plataforma através de uma reportagem e, como gosto de IA, resolvi investir. A quantidade de questões e suas análises foram tão boas que meu número de acertos foi o suficiente para entrar em Medicina na Federal do meu estado, só tenho que agradecer à equipe do AIO pela minha tão sonhada aprovação!

Jefferson, formando em Medicina
Com a plataforma AIO consegui acertar as 45 questões de ciências humanas no ENEM 2022! Sem dúvidas, obter a nota máxima nessa área, foi imprescindível para ser aprovado em medicina.


