
EsPCEx 2011
Considere o esquema a seguir, que representa uma pilha, no qual foi colocado um voltímetro e uma ponte salina contendo uma solução saturada de cloreto de potássio. No Béquer 1, correspondente ao eletrodo de alumínio, está imersa uma placa de alumínio em uma solução aquosa de sulfato de alumínio (1 mol·L-1) e no Béquer 2, correspondente ao eletrodo de ferro, está imersa uma placa de ferro em uma solução aquosa de sulfato de ferro (1 mol·L-1). Os dois metais, de dimensões idênticas, estão unidos por um fio metálico.
DADOS:
Potenciais padrão de redução (Eº red) a 1 atm e 25 ºC.
Al3+ + 3 e- → Al Eº= - 1,66 V
Fe2+ + 2 e- → Fe Eº= - 0,44 V
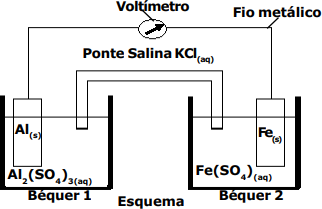
Considerando esta pilha e os dados abaixo, indique a afirmativa correta.
A placa de ferro perde massa, isto é, sofre “corrosão”.
A diferença de potencial registrada pelo voltímetro é de 1,22 V (volts).
O eletrodo de alumínio é o cátodo.
O potencial padrão de oxidação do alumínio é menor que o potencial padrão de oxidação do ferro.
À medida que a reação ocorre, os cátions K+ da ponte salina se dirigem para o béquer que contém a solução de Al2(SO4)3.
Insights de Estudo
Taxa de Acerto
Material de Estudo
Conteúdo Exclusivo
Cadastre-se para ver dicas, estratégias e análise completa desta questão
Criar conta grátis →🎓 AIO + EsPCEx: Preparação Baseada em Dados
Fizemos o trabalho difícil para você não ter que fazer
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de AI + aprendizado ativo


