
Feevale 2024/1
Células galvânicas que usam o gás hidrogênio como combustível têm sido desenvolvidas há muitos anos e já são empregadas em ônibus espaciais e protótipos de automóveis. Entretanto, esse gás é altamente inflamável. Logo, transportá-lo e armazená-lo com segurança ainda é um grande desafio.
O uso do metanol (CH3OH) como combustível tem apresentado diversas vantagens em relação ao hidrogênio, além de ser um líquido à temperatura ambiente. A figura a seguir mostra o funcionamento de uma célula a combustível de metanol, bem como a equação global do processo eletroquímico envolvido.
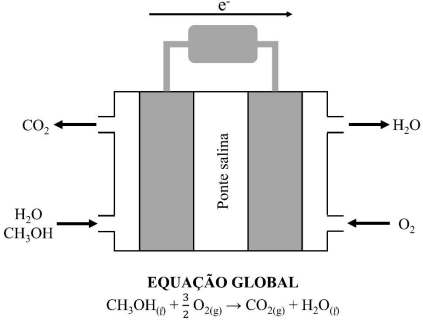
Sobre esse processo, são feitas as seguintes afirmações.
I. O gás oxigênio sofre redução no polo negativo dessa célula.
II. O número de oxidação do carbono aumenta de -2 para +4.
III. O metanol atua como agente oxidante nesse processo.
IV. O gás carbônico é produzido no ânodo dessa célula.
Marque a alternativa correta
Apenas as afirmações I e II estão corretas.
Apenas as afirmações I e III estão corretas.
Apenas as afirmações II e III estão corretas.
Apenas as afirmações II e IV estão corretas.
Apenas as afirmações III e IV estão corretas.
Insights de Estudo
Taxa de Acerto
Material de Estudo
Conteúdo Exclusivo
Cadastre-se para ver dicas, estratégias e análise completa desta questão
Criar conta grátis →🎓 AIO + Feevale: Preparação Baseada em Dados
Fizemos o trabalho difícil para você não ter que fazer
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de AI + aprendizado ativo


