
UEL 2012
1° Fase
📚
+
2.180
questões UEL
Comece sua preparação
→
UEL 2012
Baterias de íon-lítio empregam o lítio na forma iônica, que está presente no eletrólito pela dissolução de sais de lítio em solventes não aquosos. Durante o processo de descarga da bateria, os íons lítio deslocam-se do interior da estrutura que compõe o anodo (grafite) até a estrutura que compõe o catodo (CoO2), enquanto os elétrons se movem através do circuito externo (Fig. 31).
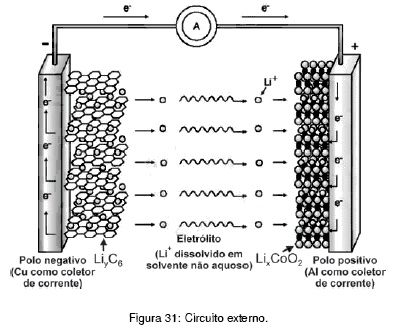
Neste processo, o cobalto sofre uma alteração representada pela equação a seguir.
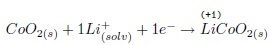
Com base no enunciado, assinale a alternativa correta.
a
Durante a descarga, o número de oxidação do cobalto aumenta.
b
O cobalto recebe elétrons, para haver a recarga da bateria.
c
No catodo, o cobalto é reduzido durante a descarga.
d
O íon de lítio se desloca para o catodo, durante a descarga, devido à atração magnética.
e
O solvente utilizado entre os polos deve ser um líquido orgânico apolar.
Resposta
C
Tempo médio
4 min
Resolução
Esta resolução não é pública. Assine a aio para ter acesso a essa resolução e muito mais:
Tenha acesso a simulados reduzidos, mais de 200.000 questões, orientação personalizada,
video aulas, correção de redações e uma equipe sempre disposta a te ajudar.
Tudo isso com acompanhamento TRI em tempo real.
Dicas
expand_more
expand_less
Dicas sobre como resolver essa questão
Erros Comuns
expand_more
expand_less
Alguns erros comuns que estudantes podem cometer ao resolver esta questão
Conceitos chave
Conceitos chave sobre essa questão, que pode te ajudar a resolver questões similares
Estratégia de resolução
Uma estratégia sobre a forma apropriada de se chegar a resposta correta
✓
Resposta Correta
C
Dificuldade
Difícil
• 37% acertaram
Tempo Médio
4min 37s
📊
Insights de Estudo
⚗️
Eletroquímica: conceitos de NOX
•
Química
Taxa de Acerto
37%
acerto
💡
Material de Estudo
🔓
Conteúdo Exclusivo
Cadastre-se para ver dicas, estratégias e análise completa desta questão
Criar conta grátis →
🎓
Vestibular
🎓 AIO + UEL: Preparação Baseada em Dados
Fizemos o trabalho difícil para você não ter que fazer
📚
2.180
questões UEL
📊
34%
cobertura de tópicos
🎯
0
alunos prep. para UEL
⭐
Depoimentos
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de AI + aprendizado ativo
+25 pts
Aumento médio TRI
4x
Simulados mais rápidos
+80 mil
Estudantes

Sarah
Aprovado
❝
Neste ano da minha aprovação, a AIO foi a forma perfeita de eu entender meus pontos fortes e fracos, melhorar minha estratégia de prova e, alcançar uma nota excepcional que me permitiu realizar meu objetivo na universidade dos meus sonhos. Só tenho a agradecer à AIO ... pois com certeza não conseguiria sozinha.

Jairo Thiago
Aprovado
❝
Conheci a plataforma através de uma reportagem e, como gosto de IA, resolvi investir. A quantidade de questões e suas análises foram tão boas que meu número de acertos foi o suficiente para entrar em Medicina na Federal do meu estado, só tenho que agradecer à equipe do AIO pela minha tão sonhada aprovação!

Jonas de Souza
Aprovado
❝
As correções de redações e as aulas são bem organizadas e é claro os professores são os melhores com a melhor metodologia de ensino, sem dúvidas contribuiu muito para o aumento de 120 pontos na minha média final!