
Prefeitura de Santa Rosa 2023
As reações de oxirredução envolvem a transferência de elétrons entre as espécies químicas, o que é evidenciado pela mudança no número de oxidação (Nox) dos participantes da reação. Observe a reação abaixo.
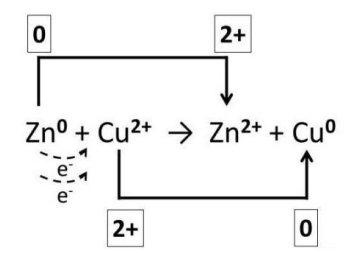
Fonte da imagem: Modificado de Mundo Educação.
Nessa reação, o Zn0 é:
O agente redutor, visto que sofre redução.
O agente redutor, visto que sofre oxidação.
O agente oxidante, visto que sofre redução.
O agente oxidante, visto que sofre oxidação.
O agente oxidante, visto que provoca oxidação.
Insights de Estudo
Material de Estudo
Conteúdo Exclusivo
Cadastre-se para ver dicas, estratégias e análise completa desta questão
Criar conta grátis →🎓 AIO + Prefeitura de Santa Rosa: Preparação Baseada em Dados
Fizemos o trabalho difícil para você não ter que fazer
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de AI + aprendizado ativo


