
PUC-PR Inverno Demais Cursos 2017
Ainda que outras fontes de energia já sejam realidade em várias regiões do mundo, os hidrocarbonetos continuam sendo uma importante forma de matriz energética, desde o aquecimento das casas até os automóveis e indústrias, a sociedade ainda se vê amarrada à utilização dessas substâncias. A tabela a seguir apresenta os calores de combustão de três hidrocarbonetos que são utilizados como combustíveis.
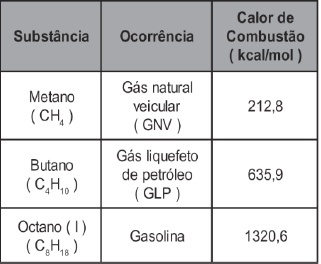
Ao analisar a relação existente entre a massa de determinada substância com o calor liberado, um engenheiro chegou à conclusão de que:
A queima de 1,0 g de butano libera cerca de 6,36 kcal.
A queima de 1,0 g de octano libera cerca de 13,20 kcal.
A queima de 1,0 g de metano libera cerca de 13,3 kcal.
A queima de 1,0 g de metano libera menos energia que a queima de 1,0 g de butano.
A queima de 1,0 g de octano libera menos energia que a queima de 1,0 g de butano.
Insights de Estudo
Taxa de Acerto
Material de Estudo
Conteúdo Exclusivo
Cadastre-se para ver dicas, estratégias e análise completa desta questão
Criar conta grátis →🎓 AIO + PUC-PR: Preparação Baseada em Dados
Fizemos o trabalho difícil para você não ter que fazer
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de AI + aprendizado ativo


