clear
UEFS 2013/1
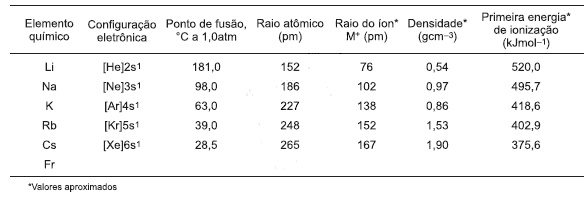
A Tabela Periódica pode ser usada para organizar e lembrar propriedades com base nos números atômicos e nas configurações eletrônicas, como o tamanho do átomo, a energia de ionização e a densidade, entre outras. Os elementos químicos em um grupo apresentam similaridades, de modo geral, mas apresentam também tendências à medida que se observam suas propriedades em um grupo ou de um grupo para outro. Algumas das propriedades físicas dos metais alcalinos são apresentadas na tabela e, a partir da análise delas, é possível verificar algumas tendências que ocorrem com os elementos químicos desse grupo da Tabela Periódica.
Uma análise dessa tabela e da Tabela Periódica dos elementos químicos permite concluir:
Uma análise dessa tabela e da Tabela Periódica dos elementos químicos permite concluir:
a
A configuração eletrônica do frâncio é representada por [Rn]7s1.
b
O frâncio é um metal alcalino gasoso, de núcleo estável, raio iônico menor que o do césio e menos reativo que o lítio.
c
A densidade desses elementos químicos mostra que seus átomos são os menores dos átomos dos metais correspondentes de cada período.
d
O tamanho do íon Li+ é muito menor que o dos demais íons dos metais alcalinos, porque, com a remoção de um elétron, a carga positiva nuclear do lítio diminui.
e
Os metais alcalinos possuem as maiores primeiras energias de ionização de cada período da Tabela Periódica e, por essa razão, são os elementos mais reativos da Tabela Periódica.
Ver resposta
Ver resposta
Resposta
A
Tempo médio
2 min
Resolução
Assine a AIO para ter acesso a esta e muitas outras resoluções
Mais de 300.000 questões com resoluções e dados exclusivos disponíveis para alunos AIO.
E mais: nota TRI a todo o momento.
E mais: nota TRI a todo o momento.
Saiba mais
Esta resolução não é pública. Assine a aio para ter acesso a essa resolução e muito mais:
Tenha acesso a simulados reduzidos, mais de 200.000 questões, orientação personalizada,
video aulas, correção de redações e uma equipe sempre disposta a te ajudar.
Tudo isso com acompanhamento TRI em tempo real.
Dicas
expand_more
expand_less
Dicas sobre como resolver essa questão
Erros Comuns
expand_more
expand_less
Alguns erros comuns que estudantes podem cometer ao resolver esta questão
Conceitos chave
Conceitos chave sobre essa questão, que pode te ajudar a resolver questões similares
Estratégia de resolução
Uma estratégia sobre a forma apropriada de se chegar a resposta correta
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de
AI + aprendizado ativo.
+25 pts
Aumento médio TRI
4x
Simulados mais rápidos
+50 mil
Estudantes

Jonas de Souza
As correções de redações e as aulas são bem organizadas e é claro os professores são os melhores com a melhor metodologia de ensino, sem dúvidas contribuiu muito para o aumento de 120 pontos na minha média final!

Murilo Martins
Com a ajuda da AIO, aumentei os meus acertos nos simulados e no ENEM, além de garantia uma TRI mais elevada. Recomendo a AIO para estudantes de todo nível, sendo uma maneira de alavancar a sua nota no menor tempo possível!

Sarah
Neste ano da minha aprovação, a AIO foi a forma perfeita de eu entender meus pontos fortes e fracos, melhorar minha estratégia de prova e, alcançar uma nota excepcional que me permitiu realizar meu objetivo na universidade dos meus sonhos. Só tenho a agradecer à AIO ... pois com certeza não conseguiria sozinha.


