PUC-RS Verão 2021
A galvanoplastia usa a eletrólise com eletrodos ativos (não inertes) para depositar uma fina camada de metal em outro. Os objetivos desse processo são refinamento de metais ou de melhorar o aspecto final ou a resistência à corrosão do metal a ser galvanizado. A figura abaixo representa uma célula eletrolítica com eletrodos ativos de cobre e uma solução aquosa de sulfato de cobre (II). A solução aquosa de íons de Cu2+ é de cor azul.
Dados: Potencial padrão de redução
Cu2+ (aq) + 2e– → Cu(s) E0red = +0,34 V
2 H2O(l) + 2e– → H2(g) + 2 OH– (aq) E0red = -0,83 V
O2(g) + 4H+ (aq) + 4e– → 2H2O(l) E0red = +1,23 V
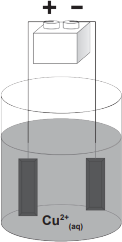
Com base na figura, são feitas as seguintes afirmações:
I. No caso de eletrodeposição de cobre, a peça a ser galvanizada deverá estar conectada no cátodo.
II. Após algum tempo de aplicação da eletrólise, a cor azul da solução de Cu2+ fica menos intensa.
III. No caso de refinamento do cobre impuro, a barra com impurezas deverá estar conectada no polo negativo da célula eletrolítica.
Está/Estão correta(s) a(s) afirmativa(s)
I, apenas.
I e II, apenas.
II e III, apenas.
I, II e III.
E mais: nota TRI a todo o momento.