
FACISB 2018
A figura mostra a montagem de um experimento no qual hidrogênio gasoso foi produzido por uma reação entre magnésio e ácido clorídrico (em excesso). O hidrogênio foi borbulhado em uma proveta totalmente cheia de água. No momento do experimento, a pressão atmosférica local era de 707 mmHg e a temperatura de 300 K.
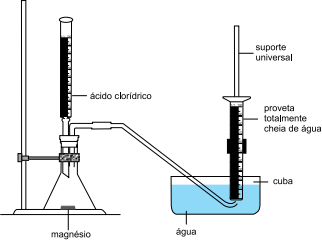
Ao final da reação, foram recolhidos na proveta 62,3 mL de uma mistura de gases constituída por hidrogênio (H2) e vapor de água.
Sabendo que a pressão de vapor de água a 300 K é aproximadamente 27 mmHg e que a constante universal dos gases, R, é igual a 62,3 L· mmHg · mol–1 · K–1, calcula-se que a quantidade de hidrogênio recolhida na proveta foi próxima de
2,3 x 10–3 mol.
3,0 x 10–2 mol.
2,3 mol.
1,1 mol.
1,1 x 10–3 mol.
Insights de Estudo
Taxa de Acerto
Material de Estudo
Conteúdo Exclusivo
Cadastre-se para ver dicas, estratégias e análise completa desta questão
Criar conta grátis →🎓 AIO + FACISB: Preparação Baseada em Dados
Fizemos o trabalho difícil para você não ter que fazer
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de AI + aprendizado ativo


