
EMESCAM 2018/2
A estrutura química a seguir é da gasolina, um hidrocarboneto de cadeia saturada e ramificada.
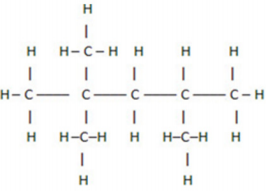
A adição de etanol (CH3CH2OH) na gasolina (C8H18), além de aumentar o índice de octanagem, viabilizando a resistência do motor, contribui ambientalmente, liberando menos monóxido de carbono para a atmosfera. Sabe-se que a porcentagem de etanol na gasolina pode variar conforme a demanda ou o mercado econômico.
O quadro a seguir mostra alguns valores arredondados das entalpias médias de ligação.
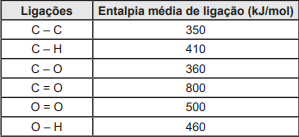
Sabe-se que a densidade do álcool e da gasolina são 0,8 g/mL e 0,7 g/mL, respectivamente, e o que percentual de álcool na gasolina é de 25% em volume.
Nessas condições, considerando que o litro da gasolina custa 4 reais, em condições ideais, qual é a energia máxima aproximada produzida quando um veículo queima gasolina comercial equivalente a um consumo de 80 reais?
250.000 kJ.
350.000 kJ.
560.000 kJ.
760.000 kJ.
Insights de Estudo
Taxa de Acerto
Material de Estudo
Conteúdo Exclusivo
Cadastre-se para ver dicas, estratégias e análise completa desta questão
Criar conta grátis →🎓 AIO + EMESCAM: Preparação Baseada em Dados
Fizemos o trabalho difícil para você não ter que fazer
Transforme seus estudos com a AIO!
Estudantes como você estão acelerando suas aprovações usando nossa plataforma de AI + aprendizado ativo


